


2020-04-22 18:31:37
团 体 标 准
2019-01-18 发布 2019-01-18 实施 东阿县阿胶行业协会 发布
T/DEXEJ 1—2019
前 言
本标准按照GB/T 1.1-2009给出的规则起草。 本标准由东阿县阿胶行业协会提出并归口。 本标准起草单位:东阿阿胶股份有限公司、山东东阿东方阿胶股份有限公司、山东东阿古胶阿 胶系列产品有限公司、山东东阿百年堂阿胶生物制品股份有限公司、山东东阿益生堂阿胶保健食品 有限公司、山东东阿东韵阿胶股份有限公司。 本标准主要起草人:周祥山、郭尚伟、段小波、贺文慧、牛伟霞、赵云峰、杨新华、雷庆涛、 陈英君、刘栋栋、桂会琳、周蕾、张海峰、孙敏。
阿胶糕
1 范围
本标准规定了阿胶糕的产品分类、原料、生产工艺、技术要求、卫生要求、试验方法、检验规则、 标志、包装、运输与贮存。
本标准适用于阿胶糕的生产、销售和检验。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文 件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 191 包装储运图示标志
GB 4789.2 食品安全国家标准 食品微生物学检验 菌落总数测定
GB 4789.3 食品安全国家标准 食品微生物学检验 大肠菌群计数
GB 4789.4 食品安全国家标准 食品微生物学检验 沙门氏菌检验
GB 4789.10 食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验
GB 4789.15 食品安全国家标准 食品微生物学检验 霉菌和酵母计数
GB 5009.3 食品安全国家标准 食品中水分的测定
GB 5009.5 食品安全国家标准 食品中蛋白质的测定
GB 5009.11 食品安全国家标准 食品中总砷及无机砷的测定
GB 5009.12 食品安全国家标准 食品中铅的测定
GB 5009.22 食品安全国家标准 食品中黄曲霉毒素 B 族和 G 族的测定
GB 5009.227 食品安全国家标准 食品过氧化值的测定
GB 5009.229 食品安全国家标准 食品酸价的测定
GB/T 6543 运输包装用单瓦楞纸箱和双瓦楞纸箱
GB 7718 预包装食品标签通则
GB 9683 复合食品包装袋卫生标准
GB 14881 食品安全国家标准 食品企业通用卫生规范
GB 19300 食品安全国家标准 坚果与籽类食品
GB/T 20977 糕点通则
GB 28050 食品安全国家标准 预包装食品营养标签通则
JJF 1070 定量包装商品净含量计量检验规则
《定量包装商品计量监督管理办法》 国家质量监督检验检疫总局[2005]第 75 号令
《中华人民共和国药典》 一部 《关于批准玛咖粉作为新资源食品的公告》 原卫生部公告 2011 第 13 号
《关于批准人参(人工种植)为新资源食品的公告》 原卫生部公告 2012 第 17 号
《关于进一步加强阿胶糕类食品生产许可工作有关问题的通知》 鲁食药监食生[2014]106 号
3 术语和定义
3.1
阿胶糕
以阿胶(含量≥10%)、黑芝麻、核桃仁为基本原料,与其他药食同源食材、普通食品原料、新食品 原料中的一种或几种(不添加黄明胶、明胶、卡拉胶以及其他具有增稠功能的食品添加剂),经原料处 理、配料、熬制、冷却、切片、包装等工序制成的产品。
4 产品分类
按使用原料不同,分为不同口味阿胶糕。如原料中添加玫瑰花,称为玫瑰阿胶糕。
5 原料
5.1 阿胶或国食健字阿胶片(块)
应符合《中华人民共和国药典》及药品补充检验方法的规定,或符合国家行政主管部门批准的相应 保健食品技术要求的规定。
5.2 核桃仁
应符合《中华人民共和国药典》或 GB 19300 的规定。
5.3 黑芝麻及其他食品原料
应符合《中华人民共和国药典》或相应标准的规定。
6 生产工艺
阿胶糕生产工艺流程包括:
a) 原料处理;
b) 配料;
c) 熬制;
d) 冷却;
e) 切片;
f) 包装;
g) 检验;
h) 入库。
7 技术要求
7.1 感官指标
应符合表 1 的规定。
表 1 感官指标

7.2 鉴别
应检出驴皮源性成分,不得检出杂皮源性(牛皮、猪皮、马皮、骡皮)成分。
7.3 理化指标
应符合表 2 的规定。
表 2 理化指标

7.4 一般微生物指标
应符合表 3 的规定。
表 3 一般微生物指标
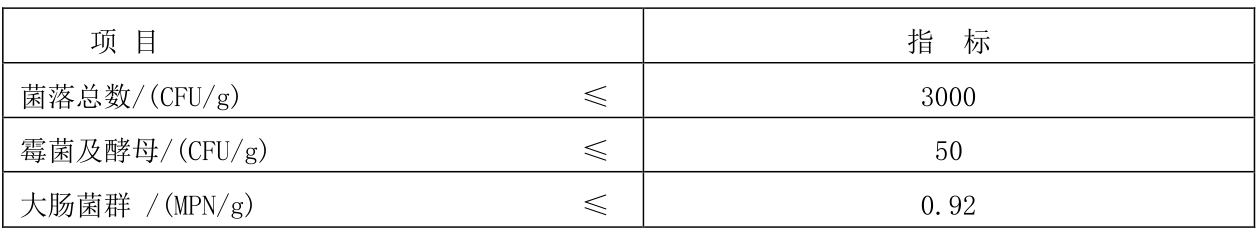
7.5 致病菌指标
应符合表 4 的规定。
表 4 致病菌指标
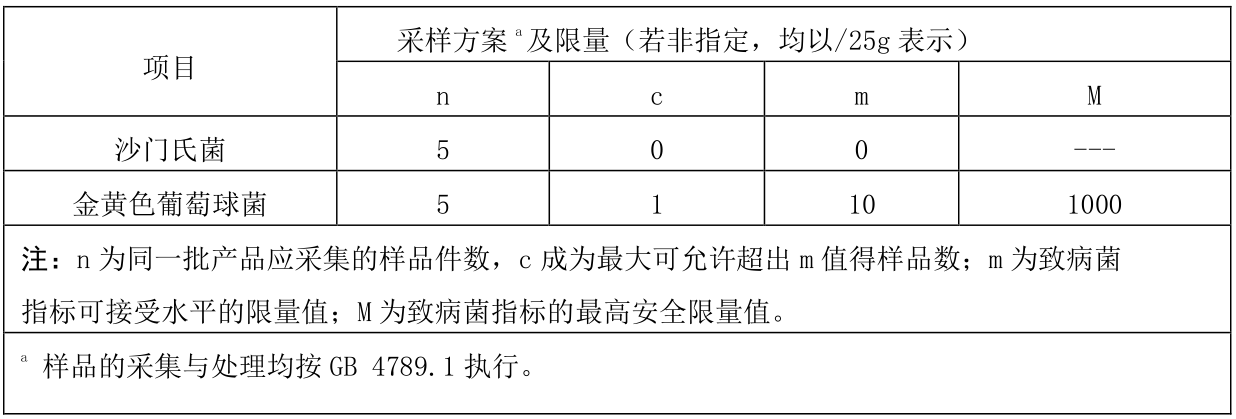
7.6 净含量
应符合国家质量监督检验检疫总局[2005]第 75 号令的规定。
8 卫生要求
卫生要求应符合 GB 14881 及鲁食药监食生[2014]106 号中加工车间的要求。
9 检验方法
9.1 感官检验
正常光线和室温条件下,目测其组织形态、色泽,嗅其气味,品尝其滋味。
9.2 鉴别
按附录 A 方法鉴定。
9.3 理化检验
9.3.1 水分
按 GB 5009.3 规定的方法测定。
9.3.2 蛋白质
按 GB 5009.5 规定的方法测定。
9.3.3 阿胶含量
按附录 B 规定的方法测定。
9.3.4 铅
按 GB 5009.12 规定的方法测定。
9.3.5 砷
按 GB 5009.11 规定的方法测定。
9.3.6 总糖
按 GB /T 20977 规定的方法测定
9.3.7 酸价、过氧化值
按 GB 5009.229、GB 5009.227 规定的方法测定。
9.3.8 黄曲霉毒素 B 1
按 GB 5009.22 规定的方法测定。
9.4 微生物检验
9.4.1 菌落总数
按 GB 4789.2 规定的方法检验。
9.4.2 大肠菌群
按 GB 4789.3 规定的方法检验。
9.4.3 霉菌及酵母
按 GB 4789.15 规定的方法检验。
9.4.4 致病菌
按 GB 4789.4、GB 4789.10 规定的方法检验。
9.5 净含量检验
按 JJF 1070 规定的方法进行。
10 检验规则
10.1 组批
同原料,同批次投料,同一生产线生产的包装完好的同一种产品为一组批。
10.2 抽样
从同一批次样品的 4 个不同部位抽取,抽样量满足不少于 5 个独立包装,且抽样量不少于 600 克。
10.3 检验
10.3.1 出厂检验
出厂检验项目包括鉴别、阿胶含量、感官指标、净含量、水分、蛋白质、菌落总数、霉菌及酵母和大肠菌群。每批产品应检验合格并签发质量合格证方可出厂。
10.3.2 型式检验
10.3.2.1 正常生产时每半年进行一次,有下列情况之一时也应进行型式检验:
——新产品投产前;
——出厂检验结果与上次型式检验有较大差异;
——更换设备、主要原辅材料或更改关键工艺可能影响产品质量时;
——停产半年及以上,再恢复生产时;
——国家行政主管部门提出进行型式检验要求时。
10.3.2.2 检验项目为本标准的规定的全部项目。
10.4 判定规则
10.4.1检验项目全部符合本标准的规定,判该批产品为合格产品。
10.4.2 微生物指标如有一项不符合要求,即判该批产品为不合格。其他项目如有一项以上(含一项)
不合格,应在同批产品中加倍抽样复验,以复验结果为准。若复验项目仍有一项不合格,则判该批产
品为不合格品。
11 标志、包装、运输、贮存
11.1 标志
产品包装储运图示标志应符合GB/T 191、GB/T 6388的规定,标签及说明书应符合GB 7718、GB 28050及相关规定。
11.2 包装
11.2.1 产品内包装材料应符合 GB 9683 的规定。
11.2.2 产品外包装为瓦楞纸箱,应符合GB/T 6543的规定。
11.2.3 包装应牢固、防潮、整洁、美观、无异气味,便于装卸、仓储和运输。
11.3 运输
11.3.1 产品运输工具应清洁无污染,运输产品时应避免日晒、雨淋,不得与有毒、有害、有异味或影响产品质量的物品混装混运。
11.3.2 搬运时应轻拿轻放,严禁扔摔、撞击、挤压。
11.4 贮存
11.4.1 产品应贮存在常温、通风、干燥的成品库中,离地离墙存放。不得与有毒、有害、有异味、易
挥发、易腐蚀的物品混储。
11.4.2 产品在本标准规定的条件下运输贮存,保质期最长不得超过12个月。
附 录 A
(规范性附录)
阿胶糕中驴皮源、牛皮源、猪皮源、马皮源(含骡皮源)成分鉴定方法
A.1 方法概要
阿胶糕试样溶解后离心除去不溶性成分,加入三氯乙酸分离蛋白,再经胰蛋白酶酶解,采用高效液
相色谱-串联质谱检测驴皮源、牛皮源、猪皮源、马皮源(含骡皮源)特征肽,利用阿胶对照药材检查
是否含有驴皮源成分,黄明胶对照药材、新阿胶对照药材、马源寡肽A分别检查是否混有牛皮源、猪皮
源、马(骡)皮源成分。
A.2 试剂和材料
A.2.1 除非另有规定,本方法所用试剂均为分析纯或以上规格,水为GB/T 6682规定的一级水。
A.2.2 乙腈:色谱纯。
A.2.3 甲酸:质谱纯。
A.2.4 三氯乙酸:分析纯。
A.2.5 碳酸氢铵:分析纯。
A.2.6 丙酮:分析纯。
A.2.7 胰蛋白酶:序列分析纯。
A.2.8 标准品:阿胶对照药材、黄明胶对照药材、新阿胶对照药材、马源寡肽A。
A.2.9 1 %碳酸氢铵溶液:取碳酸氢铵5.0 g,加水溶解并配制成500 mL,混匀后备用。
A.2.10 胰蛋白酶溶液(2 mg/mL):称取胰蛋白酶(A.2.7)2 mg,加1%碳酸氢铵溶液1 mL,临用时配
制。
A.2.11 30%三氯乙酸溶液:快速称取三氯乙酸214.3 g,加水溶解并定容至500 mL,即得。
A.2.12 阿胶基质溶液(2.0 mg/mL):精密称取0.20 g阿胶对照药材粉末于100 mL容量瓶中,加1%碳酸氢铵溶液80 mL,超声处理30 min,使样品完全溶解,用1 % 碳酸氢铵溶液稀释至刻度,摇匀。
A.2.13 黄明胶基质溶液(2.0 mg/mL):精密称取0.10 g黄明胶对照药材于50 mL容量瓶中,加1 % 碳酸氢铵溶液40 mL,超声处理30 min,使样品完全溶解,用1%碳酸氢铵溶液稀释至刻度,摇匀。
A.2.14 新阿胶基质溶液(2.0 mg/mL):精密称取0.10 g新阿胶对照药材于50 mL容量瓶中,加1 % 碳酸氢铵溶液40 mL,超声处理30 min,使样品完全溶解,用1%碳酸氢铵溶液稀释至刻度,摇匀。
A.2.15 0.1 %甲酸水溶液:取甲酸(A.2.3)1 mL用超纯水稀释至1000 mL,超声脱气后备用。
A.3 仪器和设备
A.3.1 高效液相色谱-串联质谱仪,配有电喷雾(ESI)离子源。
A.3.2 微孔滤膜:0.22 µm,水相型。
A.3.3 分析天平:感量为0.0001 g。
A.3.4 超声波清洗器。
A.3.5 高速离心机:≥8000 r/min。
A.3.6 恒温培养箱或者电热鼓风干燥箱。
A.3.7 粉碎机。
A.4 分析步骤
A.4.1 待测液的制备
A.4.1.1 称样
取试样约 50 g 置于-20℃冰箱中冷冻过夜后,置于粉碎机中粉碎至混合均匀。称取粉碎后的样品5.0 g 于 50 mL 容量瓶中,加水并超声至充分溶解,用水稀释至刻度,制得试样悬浊液。
注:对于均一性较差的样品可适当增加样品量并粉碎。
A.4.1.2 提取
取 10 mL 试样悬浊液于 3000 rpm 离心 5 min,取离心后的清液 2~5 mL(体积记为 V’),缓缓加入等体积的 30%三氯乙酸溶液(A.2.11),充分振荡混匀,4℃静置 20 min,8000 rpm 离心 5 min,弃上清,用 2 mL 冷丙酮洗涤沉淀,8000 rpm 离心 5 min 后弃丙酮清液;再用 2 mL 丙酮重复洗涤一次并弃去丙酮
清液,室温放置 10 min 挥干丙酮,制得阿胶提取物。
A.4.1.3 酶解
向阿胶提取物中加入 1 %碳酸氢铵溶液超声溶解,将溶液移入 25 mL 容量瓶内并用 1%碳酸氢铵溶液稀释至刻度。过 0.22 µm 微孔滤膜,取 400 µL 续滤液,加 40 µL 胰蛋白酶溶液(A.2.10),混匀,37 ℃恒温酶解 12 h,制得待测液。
A.4.2 混合对照品溶液的制备
取黄明胶基质溶液(A.2.13)、新阿胶基质溶液(A.2.14)各2.50 mL,并取马源寡肽A适量,置于同一50 mL容量瓶中,加阿胶基质溶液(A.2.12)并定容至刻度并摇匀,制成每1 mL阿胶基质溶液含黄
明胶、新阿胶各0.10 mg,马源寡肽A 0.20 µg的溶液。过0.22 µm微孔滤膜。取续滤液400 µL,加入40µL胰蛋白酶溶液(A.2.10),混匀,37℃恒温酶解12 h,制得混合对照品溶液。
A.4.3 仪器参考条件
A.4.3.1 液相色谱条件
液相色谱应满足以下条件:
a) 色谱柱:ZORBAX Eclipse Plus C18(1.8 µm,2.1×100 mm),或性能相当者;
b)流动相:A为含0.1%甲酸水溶液,B为乙腈,梯度洗脱,条件见表A.1;
c)流速:300 µL/min;
d) 进样量:5 µL。
表 A.1 洗脱条件
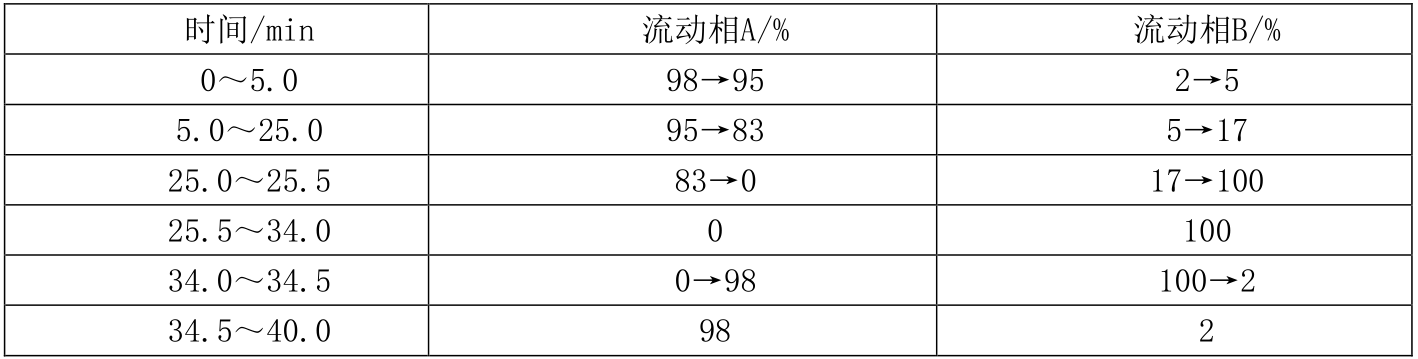
A.4.3.2 质谱条件
质谱应满足以下条件:
a) 离子源:电喷雾离子源(ESI源),选择正离子模式;
b) 扫描方式:选择离子对m/z539.8(双电荷)→m/z612.4、923.8,m/z641.3(双电荷)——726.2、783.3,m/z 774.5(双电荷)→977.8、1034.6和m/z386.3(双电荷)→m/z499.3、402.0进行多反应监测(MRM)。
A.1.1 色谱测定与峰的检出判定
按照上述条件测定待测液、混合对照品溶液,混合对照品溶液的各离子对的提取离子色谱峰的信噪比均应大于或等于10(S/N≥10)。如果待测液中同一母离子的两个离子对的色谱保留时间与混合对照品溶液相比在±2.5%的允许偏差之内,且待测液的两个离子对的提取离子色谱峰的信噪比大于或等于10(S/N≥10),则可判定为待测液中检出相应的色谱峰。
A.5 结果判定
A.5.1 驴皮源成分判定
待测液m/z539.8(双电荷)→m/z612.4、923.8提取离子流色谱中,应同时呈现与混合对照品溶液色谱保留时间一致的色谱峰。
A.5.2 牛皮源成分判定
若待测液m/z641.3—m/z726.2、783.3提取离子流图色谱中,同时出现与混合对照品溶液色谱保留时间相同的色谱峰,且样品中m/z641.3(双电荷)→m/z726.2提取离子流图中色谱峰面积超过混合对照品溶液m/z641.3(双电荷)→m/z726.2提取离子流图的峰面积K1倍,则视为含有牛皮源成分;否则,视为不含有牛皮源成分。其中K1按公式(A.1)计算:

式中:
A1 ——待测液中m/z592.0(双电荷)→m/z910.5离子流图色谱峰面积;
A2 ——混合对照品溶液中m/z592.0(双电荷)→m/z910.5离子流图色谱峰面积。
V’ ——试样离心后取用清液的体积,单位为毫升(mL);
m ——粉碎后试样的称取质量,单位为克(g)。
A.5.1 猪皮源成分判定
若待测液m/z774.5(双电荷)→977.8、1034.6提取离子流色谱图中,同时出现与混合对照品溶液色谱保留时间相同的色谱峰,且样品中m/z774.5(双电荷)→m/z977.8提取离子流图中色谱峰面积超过混合对照品溶液m/z774.5(双电荷)→m/z977.8提取离子流图的峰面积K1倍,则视为含有猪皮源成分; 否则,视为不含有猪皮源成分。其中K1按A.5.2中的公式(A.1)计算。
A.5.2 马(骡)皮源成分判定
若待测液m/z386.3(双电荷)→499.3、402.0提取离子流色谱图中,应不得同时出现与混合对照品溶液色谱保留时间相同的色谱峰;若同时出现,且样品中m/z386.3(双电荷)→m/z499.3提取离子流图中色谱峰面积超过马源寡肽A对照品溶液m/z386.3(双电荷)→m/z499.3提取离子流图的峰面积K1倍,则视为含有马(骡)皮源成分;否则,视为不含有马(骡)皮源成分。其中K1按A.5.2中的公式(A.1)计算。
附 录 B
(规范性附录)
阿胶糕中阿胶含量测定方法
B.1 方法概要
阿胶糕试样溶解后离心除去不溶性成分,加入三氯乙酸分离蛋白,再经胰蛋白酶酶解,采用高效液相色谱-串联质谱检测阿胶特征肽,利用阿胶对照药材外标法定量阿胶含量。因马皮源和骡皮源成分对阿胶含量检测有干扰,故同时采用高效液相色谱-串联质谱测定马源寡肽A,检查是否混有马(骡)皮源成分。
B.2 试剂和材料
同附录A中A.2试剂和材料。
B.3 仪器和设备
同附录A中A.3仪器和设备。
B.4 分析步骤
B.4.1 待测液的制备
同附录A 中A.4.1 待测液的制备。
B.4.2 阿胶标准工作溶液的制备
阿胶基质溶液(A.2.13)过0.22 µm微孔滤膜,分别取续滤液10、20、50、100、200、400 µL,用1%碳酸氢铵补足至400 µL,混匀,即得阿胶含量分别0.05 mg/mL、0.10 mg/mL、0.25 mg/mL、0.5 mg/mL、1.0 mg/mL、2.0 mg/mL阿胶标准系列。分别加入40 µL胰蛋白酶溶液(A.2.11),混匀,37℃恒温酶解12 h,制得阿胶标准工作溶液。B.4.3 仪器参考条件
B.4.3.1 液相色谱条件
同附录A中A.4.3.1液相色谱条件。
B.4.3.2 质谱条件
质谱应满足以下条件:
a) 离子源:电喷雾离子源(ESI源),选择正离子模式;
b) 扫描方式:选择离子对m/z592.0(双电荷)→m/z556.3、910.5和m/z386.3(双电荷)→m/z499.3、 402.0进行多反应监测(MRM);
c) 干燥气、雾化气、鞘气、碰撞气等均为高纯氮气或其他合适气体,使用前应调节相应参数使质谱灵敏度达到检测要求,毛细管电压、干燥气温度、鞘气温度、鞘气流量、喷嘴电压、碰撞能量、碎裂电压等参数应优化至最佳灵敏度。
B.4.4 色谱测定与峰的检出判定
按照上述条件测定阿胶标准工作溶液、混合对照品溶液、待测液,阿胶标准工作溶液、混合对照品溶液的各离子对的提取离子色谱峰的信噪比均应大于或等于10(S/N≥10)。如果待测液中m/z386.3(双电荷)→m/z499.3、402.0提取离子流图的色谱保留时间与阿胶标准工作溶液相比在±2.5%的允许偏差之内,且待测液的m/z386.3(双电荷)→m/z499.3、402.0的提取离子流图的信噪比大于或等于10(S/N≥10),则可判定待测液中检出m/z386.3(双电荷)→m/z499.3、402.0色谱峰。同样,如果待测液中m/z592.0(双电荷)→m/z556.3、910.5提取离子流图的色谱保留时间与阿胶标准工作溶液相比在±2.5% 的允许偏差之内,且待测液的m/z592.0(双电荷)→m/z556.3、910.5的提取离子流图的信噪比大于或等于10(S/N≥10),则可判定待测液中检出m/z592.0(双电荷)→m/z556.3、910.5色谱峰。
B.1.1 阿胶含量的定量测定
B.1.1.1 标准曲线的制作
将阿胶标准工作溶液(B.4.2)分别按仪器参考条件(B.4.3)进行测定,得到相应的标准溶液中m/z592.0(双电荷)→m/z910.5的色谱峰面积。以阿胶标准工作溶液的浓度为横坐标,以色谱峰的峰面积为纵坐标,绘制标准曲线。
B.1.1.2 试样溶液的测定
将待测液按仪器参考条件(B.4.3)进行测定,得到相应的待测液中m/z592.0(双电荷)→m/z910.5 的色谱峰面积。根据标准曲线得到待测液中阿胶的浓度,平行测定次数不少于两次,两次独立测定结果的绝对差值不得超过算术平均值的15%。
B.5 结果判定
B.5.1 马(骡)皮源成分判定
按下述条件判定是否含有马(骡)皮源成分。若含有,则不能用本方法判定该样品中阿胶的含量。若待测液中检出m/z386.3(双电荷)→499.3、402.0色谱峰,且样品中m/z386.3(双电荷)→m/z499.3
提取离子流图中色谱峰面积超过混合对照品溶液m/z386.3(双电荷)→m/z499.3提取离子流图的峰面积K1倍,则视为含有马(骡)皮源成分;否则,视为不含有马(骡)皮源成分。其中K1按公式(B.1)计算:
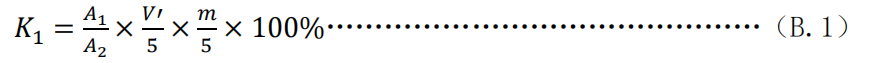
式中: A1 ——待测液中m/z592.0(双电荷)→m/z910.5离子流图色谱峰面积;
A2 ——混合对照品溶液中m/z592.0(双电荷)→m/z910.5离子流图色谱峰面积。
V’ ——试样离心后取用清液的体积,单位为毫升(mL);
m ——粉碎后试样的称取质量,单位为克(g);
B.5.2 阿胶含量的计算
当待测液中不含有马(骡)皮源成分时,试样中阿胶含量按公式(B.2)计算:
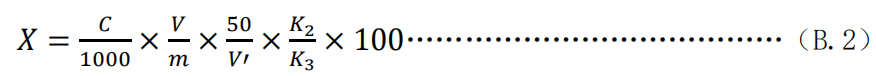
式中: X ——试样中阿胶的含量,单位为克每百克(g/100g); C ——从标准曲线中读出的待测液中阿胶的浓度,单位为毫克每毫升(mg/mL); V ——试样的最终定容体积,25 mL; V’ ——试样离心后取用清液的体积,单位为毫升(mL); m ——粉碎后试样的称取质量,单位为克(g);
K2 ——阿胶对照药材的折算系数,K2=W1÷W2,其中W1为阿胶对照药材中L-羟脯氨酸、甘氨酸、丙氨酸、L-脯氨酸的四种氨基酸含量之和,其检测方法参考中华人民共和国药典一部中阿胶含量测定项下四种氨基酸的含量测定方法;W2=43 %,为中华人民共和国药典一部中阿胶中四种氨基酸的标准含量之和;
K3 ——校正因子,即K3 = 0.75。
以两个平行试样测定结果的算术平均值报告结果,保留一位小数。
